乳がん治療の最新のトレンド
乳がん治療における最新のトレンドは、個別化治療、免疫療法、新しい薬剤の開発、そして低侵襲治療の進展に焦点が当てられています。以下、これらのトレンドを詳述します。
1. 個別化医療(Precision Medicine)
個別化医療とは、患者の遺伝情報、腫瘍の特性、患者の生活環境などを総合的に考慮し、それに基づいて最適な治療法を選択するアプローチです。乳がんにおいても、遺伝子解析を用いて各患者に適した治療を行うことが一般化しつつあります。特に、HER2陽性、ホルモン受容体陽性、トリプルネガティブ乳がんといったサブタイプごとに異なる治療法が選ばれるようになりました。
1.1 HER2陽性乳がん
HER2陽性乳がんは、従来の治療に加え、抗HER2抗体療法(例:トラスツズマブ(ハーセプチン))が標準治療として確立されており、これにより予後が大幅に改善しています。最近では、抗体薬物複合体(ADC)と呼ばれる治療法が注目されています。**トラスツズマブ デルクステカン(Enhertu)**は、その代表的な薬剤で、従来の治療が効かない患者にも効果が期待されています。
1.2 ホルモン受容体陽性乳がん
ホルモン受容体陽性の乳がんは、ホルモン療法が基本です。これに加えて、近年ではCDK4/6阻害薬が登場し、特に進行性乳がんや再発乳がんの治療において画期的な成果を上げています。代表的な薬剤として**パルボシクリブ(Ibrance)やアベマシクリブ(Verzenio)**があります。これらの薬剤は、ホルモン療法との併用により、腫瘍の増殖を抑える効果が高いとされています。
1.3 トリプルネガティブ乳がん
トリプルネガティブ乳がん(TNBC)は、ホルモン受容体もHER2も発現していないため、これまで有効な治療法が限られていました。しかし、近年では免疫チェックポイント阻害薬やPARP阻害薬などの新しい治療法が登場しています。特に**アテゾリズマブ(Tecentriq)やオラパリブ(Lynparza)**が代表的な薬剤で、特定の遺伝子変異を持つ患者に対して有望な結果を示しています。
2. 免疫療法(Immunotherapy)
免疫療法は、患者の免疫システムを活性化させてがん細胞を攻撃する治療法です。乳がんに対する免疫療法は、特にTNBCにおいて進展が著しいです。免疫チェックポイント阻害薬は、がん細胞が免疫系から逃れようとするメカニズムを阻害し、免疫細胞ががん細胞を攻撃できるようにするものです。PD-1阻害薬やPD-L1阻害薬がこのカテゴリに属し、TNBC患者に対する治療効果が確認されています。
また、CAR-T細胞療法も乳がん治療において研究が進んでいます。CAR-T細胞療法は、患者のT細胞を遺伝子改変し、特定のがん細胞を標的とする受容体を持たせることで、強力な抗がん効果を発揮する治療法です。現在、乳がんに対する臨床試験が進行中で、今後の実用化が期待されています。
3. 新薬の開発と標的療法の進展
新しい薬剤の開発は、乳がん治療において常に重要な役割を果たしています。これまでの薬剤が効かない、あるいは副作用が強い場合に、新しい薬剤が次々と登場して患者の選択肢が広がっています。
3.1 抗体薬物複合体(ADC)
抗体薬物複合体は、特定のがん細胞に結合する抗体に、細胞毒性を持つ薬剤を結合させた治療法です。これにより、がん細胞に対して選択的に薬剤を届けることが可能になり、正常細胞への影響を最小限に抑えることができます。先述したトラスツズマブ デルクステカンは、この技術を用いた治療薬です。
3.2 PARP阻害薬
PARP阻害薬は、DNA修復酵素であるPARPを阻害し、がん細胞の増殖を抑制する薬剤です。特にBRCA1やBRCA2遺伝子変異を持つ乳がん患者に効果的であり、オラパリブやタラゾパリブが承認されています。これにより、遺伝子変異に基づく治療がさらに広がりつつあります。
4. 低侵襲治療の進展
乳がん治療においては、手術や放射線治療などの身体的負担を減らすことも重要な課題です。近年では、低侵襲の外科手術技術や、より精度の高い放射線治療技術が進展しています。
4.1 乳房温存手術
乳房温存手術は、がん細胞のみを取り除き、乳房の形状や機能をできるだけ保つ手術です。従来はがんの進行度によっては乳房全体を切除する乳房全摘手術が主流でしたが、早期発見が増えたことや、術前化学療法の発展により、乳房温存手術が可能な患者が増えています。
4.2 乳房再建手術
乳房再建手術は、乳房切除後に乳房を再構築する手術で、患者のQOL(生活の質)向上に寄与しています。再建にはインプラント法や自家組織法がありますが、最近では、より自然な形状を実現するための新技術や素材の開発が進んでいます。
4.3 放射線治療
放射線治療においても、正常な組織へのダメージを最小限に抑え、がん細胞だけを標的とする技術が進化しています。特に**IMRT(強度変調放射線治療)やIGRT(画像誘導放射線治療)**といった技術が普及し、より効果的かつ副作用の少ない治療が可能になりました。
5. 総合的な治療アプローチ
乳がんの治療においては、外科手術、化学療法、放射線治療、ホルモン療法、免疫療法などのさまざまな治療法を組み合わせた集学的治療が標準的となっています。特に進行がんや再発がんに対しては、個別の治療法だけでは十分な効果が得られない場合が多いため、これらの治療法を組み合わせることで、より効果的な治療が行われています。
また、患者の心理的サポートや栄養管理、運動療法など、治療の副作用を軽減し、患者の生活の質を向上させるためのサポーティブケアも重要視されています。乳がん患者の生存率が向上する中で、QOLの維持・向上が治療の大きなテーマとなっているのです。
6. 未来の展望
乳がん治療は日々進歩を遂げており、これまで治療が困難だったタイプのがんにも有効な治療法が増えています。今後の課題としては、さらなる副作用の低減と、治療のパーソナライズ化が挙げられます。これに加え、AIを用いた診断・治療の精度向上、遺伝子治療やナノテクノロジーを活用した新しい治療法の開発など、技術革新によって乳がん治療の未来は明るいとされています。
結論
乳がん治療は、個別化医療の進展、免疫療法の導入、新薬の開発、低侵襲治療の進化といった様々なトレンドを通じて大きく前進しています。これらの進展は、患者の生存率を向上させるだけでなく、QOLの向上にも寄与しており、今後もさらなる治療法の発展が期待されています。
以上、2024年10月24日

文責 虎の門病院 乳腺・内分泌外科 川端英孝(2019年5月6日;写真は病院玄関)
【要約】ホルモン受容体とHER2(human epidermal growth factor 2)は乳癌治療における2つの主な分子標的であり、腫瘍におけるこれら分子マーカーの有無によって乳癌は3つのサブタイプに分類され薬物療法が行われる。2019年の保険適応が予想されているがんゲノム医療は従来のコンパニオン検査に代わり、遺伝子パネル検査を用い薬物療法を選択するアプローチであり、当面の治療選択への影響は少ないものの社会的なインパクトは大きいと予想される。

The Okura Tokyo Aug. 2021
はじめに
本著は放射線診断に関わる先生方に是非知っておいていただきたい乳癌治療のトレンドの紹介という意図で書かれたものである。現在の治療の根幹をなす乳癌の3つのサブタイプの話を中心に治療の現状を解説し、後半では2019年6月に保険適応とされることが予想されている「がんゲノム医療」について言及している。乳癌における「がんゲノム医療」の役割は当面限定的と考えられているが、一般社会からの注目度は高く2019年7月に東京で開催される日本乳癌学会総会(会長は埼玉医科大学国際医療センター院長・佐伯俊昭先生)においても「がんゲノム医療」は中心テーマの一つとして掲げられており、臨床医としてこのテーマについての理解を深めることは重要と思われる。
乳癌の主な2つの分子標的
日本では年間86500名(2018年予測値)の女性が新たに乳癌と診断されており、これは9%の女性が生涯のどこかの時点で乳癌と診断されることを意味している1)。乳癌の病態に関連して2つの主要な分子標的が明らかにされている。一つはestrogen receptor (ER)でこれはステロイドホルモン受容体であり転写因子である。エストロゲンにより活性化されるとERは乳癌細胞内の腫瘍形成を促進させる経路を活性化する。これと密接に関わるステロイドホルモンであるprogesterone receptor(PR)の発現もERのシグナル伝達活性化のマーカーである。ER又はPRの発現が1%でもあればホルモン受容体陽性と分類され、ERシグナル伝達をダウンレギュレートするホルモン療法が第一選択の治療となる。第二の分子標的はHER2(human epidermal growth factor 2)であり、これは細胞表面に存在する糖タンパクで受容体型チロシンキナーゼである。これは上皮成長因子受容体に類似した構造を持ちこの遺伝子が増幅又は過剰発現した乳癌はHER2陽性と分類され、抗体又は低分子阻害剤を用いた抗HER2療法の適応となる2)。
乳癌の3つのサブタイプと薬物療法
乳癌はホルモン受容体(ER、PR)及びHER2の分子マーカーの有無により、3つの主なサブタイプに分類されており、ホルモン受容体陽性・HER2陰性群(約70%)、HER2陽性群(15~20%)、トリプルネガティブ即ち3つのマーカーがすべて陰性の群(約15%)の3群に分けられている3)。乳癌と診断される患者さんの90%以上は初回診断時に遠隔転移は認めず、この方たちの治療目標は病気を完治させることである。トリプルネガティブ乳癌は他の2つのサブタイプに比べると再発のリスクは高く、例えば病期1期の5年生存率(5-year breast cancer-specific survival)は85%であるのに対して、他の2つのサブタイプは94~99%である。遠隔転移を有さない乳癌患者さんの薬物療法は原発巣のサブタイプによって決められ、ホルモン受容体陽性の乳癌にはホルモン療法を行い、一部の患者さんには化学療法も行う。HER2陽性の患者さんはHER2をターゲットとした抗体や低分子阻害剤を用いた療法に化学療法を併用して行う。トリプルネガティブ乳癌の患者さんには化学療法のみを行う4)。
外科手術療法
標準的なアプローチは、切除断端を陰性にした上で乳房切除(全摘)あるいは乳房部分切除+放射線照射を行うことで、標準的なアルゴリズムに従えばいずれの方法も再発率、生存率に差がないことが明らかになっている5)。腋窩リンパ節の扱いは乳房とは別の観点で考えられており、臨床的に明らかなリンパ節転移を認めた場合は郭清が選択されるが、そうでない場合はセンチネルリンパ節生検が選択される。病理組織学的に転移を認めなければ非郭清で対処するが、転移を認めた場合の対応についての詳細はいまだ議論のある課題である6)。その他術前療法が奏功した場合に臨床的に明らかだったリンパ節転移をどう扱うかなど細部の課題は残されている。
放射線療法
乳房温存手術後の乳房照射は標準と考えられており、50Gy/25分割が選択されてきた5)。近年では寡分割照射、例えば42.5Gy/16分割がこれまでの方法と同等の臨床的な結果が得られたとされ、より望ましい治療法として受け入れられている7)。乳房切除後の補助照射は腫瘍径の大きい症例、リンパ節転移の多い症例、グレードの高い腫瘍がその適応とされており、腫瘍床へのブースト照射の是非、高齢者に対する乳房温存療法後の放射線治療の省略などとともに症例毎の対応が必要となる。
進行乳癌の治療
遠隔転移を伴う乳癌もサブタイプに応じて治療されるが、そのゴールは延命と症状の緩和である。トリプルネガティブ乳癌の遠隔転移後の生存期間が1~2年であるのに対して、他の2つのサブタイプは5年前後とされており、適応となる薬剤の相違だけではなく、リスクプロファイルの明確な違いを前提とした対応が必要になる。なおこれまで乳癌の遠隔転移に完治は望めないとされてきたが、転移が限られた症例(オリゴ転移)やHER2陽性のサブタイプでは10年以上の長期にわたってCR(完全寛解)が維持されることが散見され薬物療法の進歩、診断学の進歩、照射技術の進歩などと合わせて一律に遠隔転移は完治せずを前提にしてよいかという臨床上のジレンマがある8)。
生殖細胞遺伝子変異と薬物療法選択
乳癌において遺伝子変異を標的とした治療で臨床的な効果が示されている生殖細胞変異はBRCA1/2の病的変異のみである。これらは癌抑制遺伝子でありDNAのダメージ修復の機能を有し、これらの病的変異は全乳癌の5%程度を占める。BRCAの機能不全の腫瘍に対してはPARP阻害剤が合成致死というメカニズムを介して効果を示す。オラパリブというPARP阻害剤が日本でも保険適応となっている
「がんゲノム医療」について
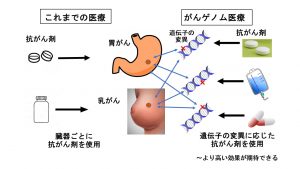
ゲノム(genome)とは、geneとome(すべてを意味する)を合わせた造語で、遺伝情報全体を表す言葉である。腫瘍組織から多数の遺伝子を同時に調べて個々の患者により効果の可能性の高い薬物療法を行うことが現時点での「がんゲノム医療」の定義である。具体的には腫瘍組織を用いて数十~数百の遺伝子を一度に調べる「がん遺伝子パネル検査」を行い、遺伝子の変異を解析する。これらは次世代シークエンサーという技術によって可能になった検査である。癌全体で見ると検査を受けた方の6割程度に治療候補薬剤が想定できる変異が見つかり、さらに適した薬物療法が提案できる可能性は治験・未承認薬も含め10~20%程度とされており、乳癌患者さんに具体的な薬剤が提案できる可能性はさらに低いと予想されている。しかしながら、これまでの医療が臓器別に薬剤治療を検討していたのに対して、遺伝子の変異毎に薬剤治療を検討するというパラダイムシフト(図1を参照)が起きていることには大いに注目に値する9)。
これまでも一個ずつ腫瘍のタンパクの発現、遺伝子の増幅を調べて(コンパニオン検査)、薬剤適応の根拠としてきたわけではあるが、これらとこれから始まる遺伝子パネル検査の違いを表1に示す。2019年6月にシスメックスの「OncoGuide NCC オンコパネルシステム」と中外製薬の「FoundationOne CDx がんゲノムプロファイル」の2つがまず保険適応とされる見通しであるが、現状では進行癌で標準的な治療をすべてやり終えた方、あるいは原発不明癌がその検査対象とされている。しかしアメリカでFoundationOne CDxは病期Ⅲ、Ⅳを対象としており、我が国の遺伝子パネル検査もいずれは適応拡大されていくものと思われるが、現状では標準治療を上回るだけの根拠はなく、すべて臨床試験の枠内で行うべきとされている2),10)。
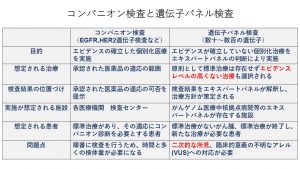
コンパニオン検査とがん遺伝子パネル検査の比較について
おわりに
乳癌は3つの主なサブタイプにより明確に分けて考えられており、それぞれのリスクプロファイルと適応となる薬物療法が明らかになっている。現在の乳癌治療はこのサブタイプと解剖学的な進行度(病期)に基づいてなされており、「がんゲノム医療」が導入されても当面の治療自体に大きな変化はないと思われるが、全く新たな視点で癌治療を捉えること で今後の発展が期待されている。
参考文献
1) https://ganjoho.jp/public/index.html
2) Waks AG, Winer EP. JAMA. 2019 ,321(3):288-300
Breast Cancer Treatment: A Review.
3) Howlader N, Altekruse SF, Li CI, et al. J Natl Cancer Inst. 2014;106(5)
US incidence of breast cancer subtypes defined by joint hormone receptor and HER2 status.
4)Breast Cancer. National Comprehensive Cancer Network: National Clinical Practice Guidelines in Oncology. Version 3. 2018. https://www.nccn.org/professionals/physician_gls/pdf/breast.pdf.
5)Fisher B, Anderson S, Bryant J, et al. N Engl J Med. 2002;347(16):1233-1241
Twenty-year follow-up of a randomized trial comparing total mastectomy, lumpectomy, and lumpectomy plus irradiation for the treatment of invasive breast cancer.
6)Giuliano AE, Hunt KK, Ballman KV, et al. JAMA. 2011;305(6):569-575.
Axillary dissection vs no axillary dissection in women with invasive breast cancer and sentinel node metastasis: a randomized clinical trial.
7)Whelan TJ, Pignol JP, Levine MN, et al. N Engl J Med. 2010;362(6):513-520.
Long-term results of hypofractionated radiation therapy for breast cancer.
8)Sledge GW Jr. J Oncol Pract. 2016 Jan;12(1):6-10.
Curing Metastatic Breast Cancer.
9) Mano H. Cancer Discov. 2012 Jun;2(6):495-502
ALKoma: a cancer subtype with a shared target.
10) Goldberg KB, Blumenthal GM, Pazdur R. Cancer J. 2018 May/Jun;24(3):131-135.
The First Year of the Food and Drug Administration Oncology Center of Excellence: Landmark Approvals in a Dynamic Regulatory Environment.
